
体重の約13分の1の重さに相当する量の血液が体の隅々まで循環しています。血液の中には液体成分(血漿)と細胞成分(赤血球、白血球と血小板)があります。血液は採血後に放っておくと固まる(凝固する)性質があり、この現象はフィブリノーゲン(線維素原)がフィブリン(線維素)となることが原因で、血小板も関係しています。固まった血液を遠心して分離すると、フィブリンと血球が下に沈んで上に血清が残ります。
血漿は体の各臓器に栄養分を運搬し、老廃物を回収しています。赤血球は酸素を組織に運び、炭水化物と脂肪の燃焼(“代謝”といいます)を助けています。白血球は細菌などの外敵を取り除き、抗体を作って同じ病原体に二度と感染しないための免疫反応に、重要な役割をしています。
出血や手術にさいして血液が失われたときに、血液型が合った血液を輸血する必要が生じます。いろいろな病気が原因で、血漿タンパクや血球が作れなくなる状態では、足りない血漿成分あるいは血球だけを輸血する必要が生じます。これを「成分輸血」と言っています。
血液の中には、体に必要な全ての成分が含まれているのです。分析してわかっている成分以外にも、まだまだ未知の重要な成分が沢山含まれているに違いありません。血漿を「魔法のジュース」といっていた偉い医学者がいましたが、血液に代わるものはないだろう、という考えを端的に表しています。
現在でも輸血は医療の中で、それに代わるものがない貴重な治療法となっていますし、将来もそうあり続けることでしょう。しかし、輸血・血液に病原体が含まれていれば受血者を感染させる、という困った事態が起こりえるのです。
輸血の歴史
古くから血液が失われると、体が次第に弱り死に至ることが知られていました。しかし、実際に輸血が行われるようになってから、まだ100年もたっていません。輸血を実現するために二つの重要な発見が必要でした。そのひとつが「血液型」で、もうひとつが血液を凝固しないようにできる「抗凝固剤」の開発でした。
1900年になってオーストリアのランドシュタイナーが血液型にA、B、Oの三つがあることを発見し、翌年に彼の弟子であるカステロが第四の血液型であるAB型を発見しました。血液型を合わせた輸血を行えば、副作用として起こる溶血を予防できることがわかったのです。1940年にランドシュタイナーとウィーナーが、もう一つの重要な血液型であるRh式血液型を発見し、現在の体制が整いました。
フィブリノーゲンがフィブリンになる血液凝固の過程で、カルシウム・イオンが必要です。ですから、採血した血液にカルシウムと結合して溶けなくするクエン酸ナトリウムを加えると、血液が凝固せず、従って輸血できることが1914年にわかり、1937年に世界で最初の血液銀行が米国のシカゴに設立されました。その後抗凝固剤が改良され、現在使用されているものに近づきました。
この頃から世界は第二次世界大戦の混乱に突入しました。戦争では兵隊さんが怪我をして出血しますから、頻繁に輸血の必要性がおこりました。そこで問題が生じました。輸血後に、黄疸を発症して肝臓が悪くなる人が出てきたのです。経口感染する「流行性」肝炎と区別するために、輸血後肝炎は「血清」肝炎と呼ばれるようになりました。
輸血後ウイルス肝炎・予防法の変遷
日本では、戦後の混乱期から1960年代の初めにかけて、輸血を受けた患者さんの約半数に肝炎が発症する、という悲惨な状況が続きました。輸血後肝炎の頻度が高かった最大の原因は「売血」制度でした。売血を職業としていた人々の間に、覚醒剤(“メタンフェタミン”で「ヒロポン」ともいいます)の静脈注射が蔓延していたのです。売血をすると赤血球が減りますから、貧血になりその治療の目的で鉄分を静脈注射して補給する必要が生じます。これら二つの理由で、売血を職業とする特殊な集団の間で汚染された注射器と注射針を使った「回し打ち」が広まり、これによって彼らの間で急激に肝炎ウイルス感染が拡散しました。そのため、売血中に肝炎ウイルスが高頻度で含まれることになってしまったのです。
当時は全くわかりませんでしたけれども、振り返ってみるとその原因は持続感染し、血液によって伝染するB型肝炎ウイルスとC型肝炎ウイルスでした。この二つの肝炎ウイルスには大きな違いがあります。日本では母児感染がB型肝炎ウイルス持続感染を起こす主な感染経路で、当時は国民の2%くらいが感染し輸血後肝炎の一因となっていたと考えられます。でも、B型肝炎ウイルスが成人に感染した場合には殆ど一過性で6ヶ月以内に治癒しますから、売血者の中に持続感染は少なかったと考えられます。逆にC型肝炎ウイルスに感染すると70%もの人に持続感染を起こしますので、効果的に売血者の間に広まったと思われます。ですから、50%以上の頻度で発生した輸血後肝炎の大部分は、C型肝炎ウイルスが原因だったろうと想像できます。
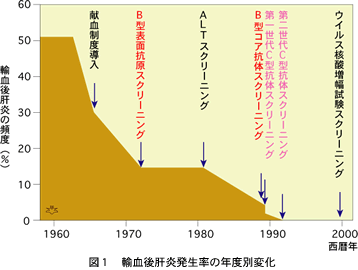 図1で、日本において輸血後肝炎が征服された輝かしい歴史をご覧ください。売血による輸血後肝炎の蔓延が明らかとなって、1964年に閣議決定により全ての採血と血液の供給が、日本赤十字社を中心とする献血で行われることになりました。その効果はめざましく、輸血後肝炎は激減しました。1972年からはB型肝炎ウイルス表面抗原であるオーストラリア抗原(「第二話
」をご覧ください)を免疫学的に測定するスクリーニングが導入され、1989年以来はB型肝炎ウイルスに持続感染していると抗体値が高くなる「B型肝炎ウイルスコア抗体」の定量によるスクリーニングが始められ、輸血後B型肝炎は事実上消滅しました。
図1で、日本において輸血後肝炎が征服された輝かしい歴史をご覧ください。売血による輸血後肝炎の蔓延が明らかとなって、1964年に閣議決定により全ての採血と血液の供給が、日本赤十字社を中心とする献血で行われることになりました。その効果はめざましく、輸血後肝炎は激減しました。1972年からはB型肝炎ウイルス表面抗原であるオーストラリア抗原(「第二話
」をご覧ください)を免疫学的に測定するスクリーニングが導入され、1989年以来はB型肝炎ウイルスに持続感染していると抗体値が高くなる「B型肝炎ウイルスコア抗体」の定量によるスクリーニングが始められ、輸血後B型肝炎は事実上消滅しました。
その結果として、以前から輸血後肝炎の主な原因であったC型肝炎ウイルスの存在が明るみに出てきました。感染者では肝機能障害があることが多いので、ALT(“GPT”とも云います)のスクリーニングが始められました。B型肝炎ウイルスコア抗体のスクリーニングも、間接的に輸血後C型肝炎の減少に役立ちました。C型肝炎ウイルスに感染している人は、以前B型肝炎ウイルスにも感染していた可能性が高いことが、その理由です。
C型肝炎ウイルス感染を特異的に発見できるようになったのは、1989年以降で、これは感染者の血液中にC型肝炎ウイルスに対する抗体が生じることを利用しています。世界に先駆けて、C型肝炎ウイルス抗体によるスクリーニングは先ず日本で始められました。でも、実はこの時点で輸血後C型肝炎の頻度は、すでに数パーセントにまで減少していたのです。1992年にC型肝炎ウイルス抗体の測定法が改良され、それを使ったスクリーニングが開始されて以来、輸血後C型肝炎の頻度はごくごくわずかになったのです。
肝炎ウイルスに感染してから血清学的診断ができるまでの潜伏期
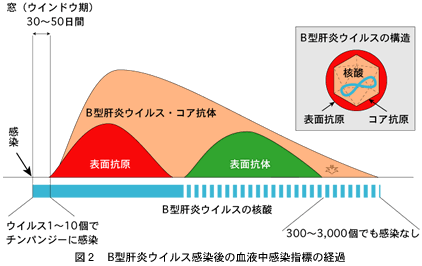 1992年までのB型肝炎ウイルスおよびC型肝炎ウイルスのスクリーニングは、全て免疫学的な方法を使って抗原または抗体を測定していました。でもこの方法ですと、感染性がある血液を見落とす危険がわずかにあるのです。ウイルスに感染してから、抗原あるいは抗体の測定によって感染を検出できるまでにB型肝炎ウイルスでは約30〜50日、C型肝炎ウイルスではもっと短く約8〜10日の「窓(ウインドウ)」といわれている期間があるためです(図2と図3)。都合の悪いことに、この期間には免疫反応がまだ始まっていませんから、とても生きの良いウイルスだけが血液中に存在します。この時期の感染は、ウイルスの核酸をPCR(polymerase
chain reaction)で増幅して測定することによって証明され、この方法を核酸増幅試験(NAT [nucleic acid amplification
test])と呼んでいます。
1992年までのB型肝炎ウイルスおよびC型肝炎ウイルスのスクリーニングは、全て免疫学的な方法を使って抗原または抗体を測定していました。でもこの方法ですと、感染性がある血液を見落とす危険がわずかにあるのです。ウイルスに感染してから、抗原あるいは抗体の測定によって感染を検出できるまでにB型肝炎ウイルスでは約30〜50日、C型肝炎ウイルスではもっと短く約8〜10日の「窓(ウインドウ)」といわれている期間があるためです(図2と図3)。都合の悪いことに、この期間には免疫反応がまだ始まっていませんから、とても生きの良いウイルスだけが血液中に存在します。この時期の感染は、ウイルスの核酸をPCR(polymerase
chain reaction)で増幅して測定することによって証明され、この方法を核酸増幅試験(NAT [nucleic acid amplification
test])と呼んでいます。
 B型肝炎ウイルスの場合ですと、ウインドウ期から採取したウイルスの僅か1〜10個だけチンパンジーに静脈注射しても、感染させることができます。表面抗原が血液中にある期間は、B型肝炎ウイルスが持続感染しています。表面抗原が消失して、表面抗体ができ、やがてコア抗体だけが検出されるようになっても、血液の中には微量のB型肝炎ウイルスが存在し続けます。この時期のB型肝炎ウイルスは、ウインドウ期と比べて感染性がずっと低く、数千個を静脈注射した場合にも、チンパンジーに感染は起こりません。多分、ウイルスに中和抗体がついていて、そのため肝臓に到達する以前に網内系(“異物”を食べる細胞がいる所です)によって血液中から除去されてしまうためだろうと思われます。
B型肝炎ウイルスの場合ですと、ウインドウ期から採取したウイルスの僅か1〜10個だけチンパンジーに静脈注射しても、感染させることができます。表面抗原が血液中にある期間は、B型肝炎ウイルスが持続感染しています。表面抗原が消失して、表面抗体ができ、やがてコア抗体だけが検出されるようになっても、血液の中には微量のB型肝炎ウイルスが存在し続けます。この時期のB型肝炎ウイルスは、ウインドウ期と比べて感染性がずっと低く、数千個を静脈注射した場合にも、チンパンジーに感染は起こりません。多分、ウイルスに中和抗体がついていて、そのため肝臓に到達する以前に網内系(“異物”を食べる細胞がいる所です)によって血液中から除去されてしまうためだろうと思われます。
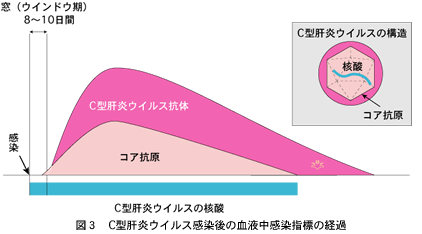
C型肝炎ウイルスは、C型肝炎コア抗原を免疫学的に測定することによっても血液中の存在を証明できますが、この方法はまだスクリーニングに加えられていません。感度が十分に高くないので、ウインドウ期の前半にはC型肝炎コア抗原が陰性でも核酸増幅試験によっては感染を発見できる時期があります。
核酸増幅試験による究極の輸血後肝炎予防
1999年以来、ウインドウ期のB型肝炎ウイルスとC型肝炎ウイルス感染を発見するために、核酸増幅試験(NAT)によるスクリーニングが導入されて、輸血後肝炎の危険性がますます減少しました。このおかげで、輸血が非常に安全になりました。核酸増幅試験の対象としてHIVの核酸も同時に測定されているので、とても安心です。HIV感染にも肝炎ウイルスと同じように、感染直後に抗体では感染を発見できない「ウインドウ期」があるからです。
現在では考えられる最高の技術を駆使して、輸血後肝炎の予防が行われています。しかしどの方法によっても、輸血後肝炎を完全になくすことは理論的に難しいのです。肝炎ウイルス感染は、ウインドウ期で生きのいいウイルスが1個だけ静脈内に注射された場合でも起こりえます。10個でしたら、ほぼ間違いなく感染するでしょう。しかし、肝炎ウイルスをたった1個でも輸血・血液から排除することは不可能です。なぜなら、輸血する血液のごく一部でしか、検査ができないからです。全部を検査していたら、患者さんに点滴する血液がなくなってしまいます。
もう一つの原因は、核酸増幅試験によるウイルス検出の感度に限界があることです。1ミリリットルあたり少なくとも約100個の肝炎ウイルスがいないと、陽性の結果が出ないのです。ですから、核酸増幅試験を含めた現在のスクリーニングの結果が全て陰性である血液の中に、絶対に肝炎ウイルスがいないと保証することは、現実的に不可能といえます。でも、その危険はごく少なく、飛行機に乗って、それが不慮の事故に遭うよりはずっと安全です。宝くじの一等賞に当たるより、もっと確率が少ないでしょう。輸血が必要になる患者さんには、それなりの重大な理由がある筈ですし、もし輸血ができないと生命が危険である状況も多いのです。輸血の恩恵と比べれば、現在の輸血後肝炎発症の危険性は無視して良いほど少なくなっている、といってよいのではないでしょうか。
輸血後肝炎をゼロにするためには、献血する方々の自覚と協力を得る以外に方法はないのです。B型肝炎ウイルスにしても、C型肝炎ウイルスにしても、ちょっとやそっとの理由では感染しません。両方とも汚染された針と注射器を使って静脈内薬物(いわゆる麻薬)の回し打ちをするか、B型肝炎ウイルスでしたら感染者と性的接触をしなければ、感染することは先ずあり得ないのです。過去にその経験がある人が献血しなければ、肝炎ウイルスのウインドウ期に感染している人を除外できますから、輸血後肝炎は完全に消滅します。勿論、献血をされる人には、あらかじめ質問表で過去の肝炎ウイルスとHIV感染の可能性を聞いています。それを良心的に申告することで、この問題は解決できる筈です。
「輸血後」肝炎と「輸血に伴う」肝炎のちがい
輸血後肝炎は「輸血後1週から6ヶ月までの間に、少なくとも2回以上の肝機能検査で血清GPT(ALT)の値が正常上界の2.5倍以上となる」ことで便宜的に定義されています。しかし輸血には、冤罪をかぶりやすい宿命があります。輸血を受けた人は、その事実をずっと覚えていますので、その直後でもずっと後にも肝炎が起こると、輸血のせいにされやすいのです。
一方で、輸血を受ける患者さんは必ずその理由があり、しかも入院しています。ですから、たとえ輸血を受けなかったとしてもほかの理由で「輸血後肝炎」の定義を満たす肝障害を発症する可能性がないとはいえません。また、ごくごくまれでしょうが、病院内での医療行為を通じて他の患者さんから、あるいは医療従事者から肝炎ウイルスが感染する危険がないとは云いきれません。特に透析を受けている腎不全の患者さんの間では、肝炎ウイルス感染の危険が高いことが知られています。
輸血が肝炎ウイルス感染の原因であることを証明する科学的方法があります。輸血後にB型肝炎あるいはC型肝炎がおこったとき、感度を上げるために保存しておいた献血者血清の量を増やして核酸増幅試験を行ってみたら、陽性の結果が得られることが、絶対にないとはいえません。また、あらゆる検査で発見できないウインドウ期にあった献血者でも、時間をおいて再検査すればウイルス感染を発見できます。しかし、いかなる場合にも輸血・血液中と患者さんの血液中にいるウイルスが同一であることを証明する必要があります。肝炎ウイルスの一つ一つが微妙に違っているために、まるで指紋のように特有な塩基の配列を調べることによって、同一のウイルスが感染したかどうかを特定することができるのです。仮に輸血後にウイルス肝炎が起こったとしても、塩基配列を調べて、それが一致した場合にだけ輸血が原因であったと確証する必要があります。そうしないと、過去40年の輝かしい輸血後肝炎制覇の歴史と、献血者を含め、それを可能とされた多くの方々の努力に対して、あまりにも不公平にならないでしょうか。
もう一度上記の図1をご覧ください。現在、年間約600万人の献血者がいて、約150万人の患者さんの治療につかわれています。これに1960年代の輸血後肝炎の発生率を適用すれば、70万人以上もの患者さんが輸血後肝炎を発症することになります。現在の優れたスクリーニングによって、輸血後ウイルス性肝炎の頻度は限りなくゼロに近づきました。その上、たとえ輸血後にウイルス肝炎が発症しても、現在はいろいろな優れた治療法で対処することができるのです。
![]()